Einnistung (Nidation)
Die Implantation (Nidation) ist der Vorgang, bei dem sich ein befruchtetes Ei in die Gebärmutterschleimhaut einbettet, damit sich ein Embryo und eine Plazenta bilden können. Sie findet normalerweise etwa 6–10 Tage nach dem Eisprung statt, wenn sich der Blastozyst anhaftet, anlegt und dann in das Endometrium eindringt. Zellen und Signalmoleküle koordinieren die Trophoblasteninvasion, die Dezidualisierung des Endometriums, die Umgestaltung der Blutgefäße und die Immuntoleranz. Sie könnten leichte Schmierblutungen oder Krämpfe bemerken, aber eine Schwangerschaft wird durch Tests bestätigt; lesen Sie weiter, um mehr über Zeitpunkt, Anzeichen, Ursachen und Behandlungsmöglichkeiten zu erfahren.
Was ist die Einnistung (Nidation)?
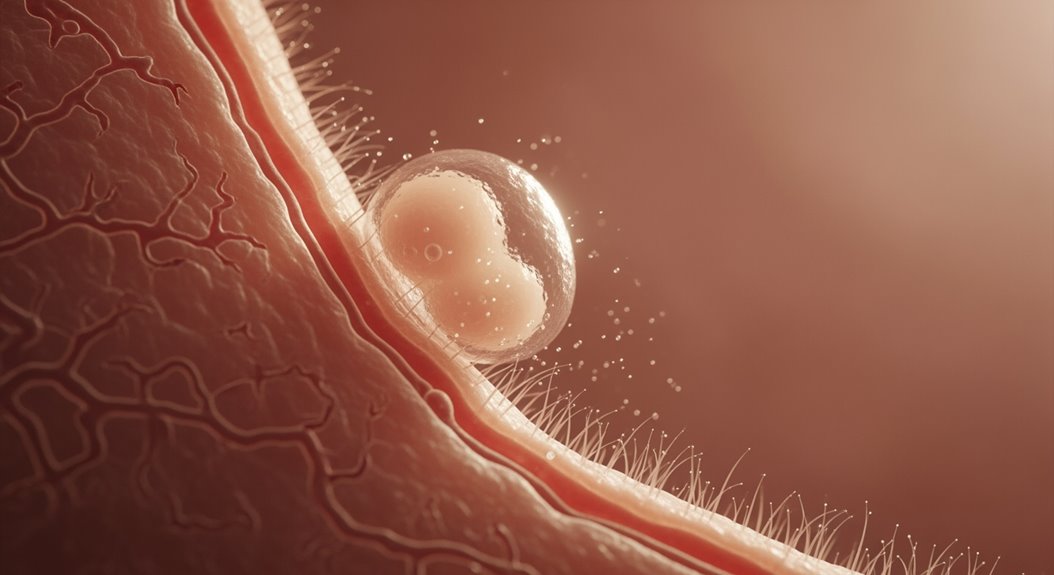
Die Implantation, auch Nidation genannt, ist der Prozess, bei dem sich ein befruchtetes Ei in die Schleimhaut Ihrer Gebärmutter einbettet, damit es sich zu einem Embryo entwickeln kann. Der Begriff Implantationsprozess beschreibt, wie der Blastozyst — eine winzige Zellkugel — die Gebärmutterschleimhaut berührt, Signale an das Gewebe sendet und mit der Embryo-Anheftung beginnt. Zunächst werden Sie keine dramatischen Veränderungen verspüren; biochemische Kommunikation steuert Adhäsion, das Eindringen von Endometriumzellen und die Etablierung des Nährstoffaustauschs. Ihre Gebärmutterschleimhaut wird empfänglich und produziert Faktoren, die dem Embryo das Anhaften und den Beginn der Plazentabildung ermöglichen. Die äußeren Zellen des Embryos remodeln das mütterliche Gewebe, wodurch sich eine Blutversorgung entwickelt und das frühe Wachstum unterstützt wird. Sie könnten leichte Schmierblutungen oder Krämpfe bemerken, aber viele Menschen sind sich dieses Schrittes nicht bewusst. Das Verständnis der Implantation hilft Ihnen zu erkennen, dass Frühschwangerschaft ein koordiniert ablaufender zellulärer Dialog und kein einzelnes Ereignis ist, wobei das erfolgreiche Anhaften des Embryos die entscheidende Verschiebung vom befruchteten Ei zum sich entwickelnden Embryo darstellt.
Zeitpunkt und Stadien der Einnistung

Obwohl es sich plötzlich anfühlen kann, folgt der Eintritt des Embryos in die Gebärmutterschleimhaut einem vorhersehbaren Zeitplan: Nach der Befruchtung in den Eileitern wandert der sich entwickelnde Blastozyst in Richtung Gebärmutter und beginnt sich typischerweise etwa 6–10 Tage nach dem Eisprung anzulagern, wobei die vollständige Invasion und die Anlage der Plazenta etwa um Tag 12–14 abgeschlossen sind. Sie werden die Implantationszeit oft durch klare Implantationsphasen erklärt sehen: Apposition (lose Kontaktaufnahme), Adhäsion (stabile Anlagerung) und Invasion (Einnistung in das Endometrium). Etwa an den Tagen 6–7 können Sie Apposition und erste Adhäsion erwarten, während sich die Blastozyste an die rezeptive Oberfläche ausrichtet. In den Tagen 8–10 wird die Adhäsion stärker und Sie können subtile Anzeichen wie leichte Schmierblutungen bemerken. Ab etwa Tag 10 proliferiert, differenziert und invasiert der Trophoblast und etabliert die frühe Plazenta sowie die mütterliche Blutkommunikation bis zu den Tagen 12–14. Das Wissen um diese Phasen hilft Ihnen, frühe Symptome und den Zeitpunkt für Tests einzuordnen, und erklärt, warum implantationsbedingte Veränderungen in einem engen, vorhersehbaren Fenster auftreten.
Zelluläre und molekulare Mechanismen
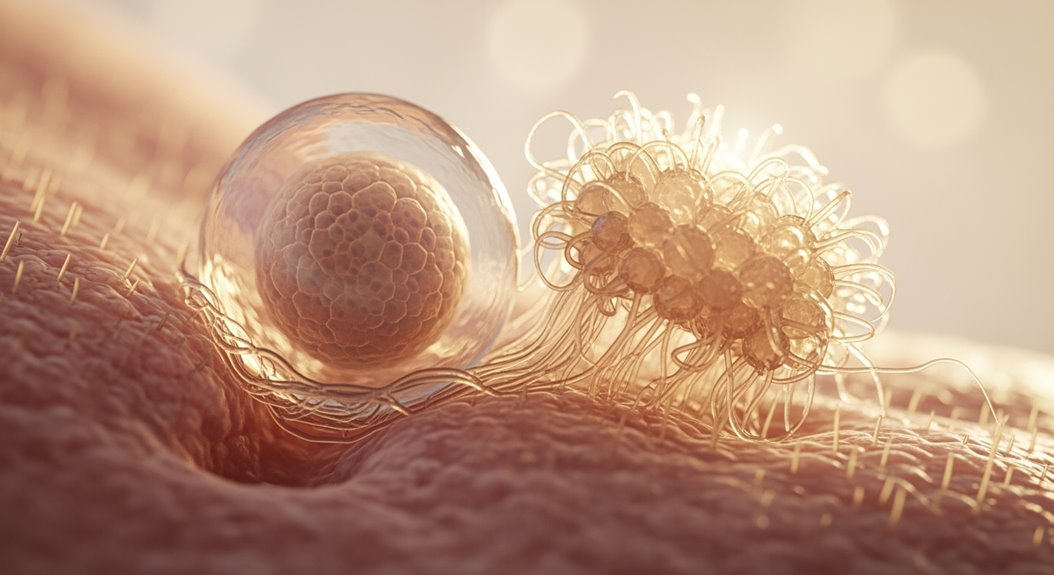
Weil die Einnistung (Implantation) von eng koordinierten Zellverhalten und Signalen abhängt, bedeutet das Verständnis des Prozesses, sowohl die Blastozyste als auch das Endometrium auf molekularer Ebene zu betrachten. Sie werden sehen, wie die Trophoblastzellen der Blastozyste anhaften, in mütterliches Gewebe eindringen und es umgestalten, geleitet von Adhäsionsmolekülen, Proteasen und lokalisierten Zell-Signalen. Die innere Zellmasse bewahrt die Pluripotenz, während nahegelegene stammzellähnliche Zellen durch Veränderungen der Genexpression mit der Differenzierung in verschiedene Zelllinien beginnen. Sie sind auf Zytokine, Wachstumsfaktoren und integrinvermittelte Kontakte angewiesen, um die Trophoblastinvasion mit mütterlichen Reaktionen zu synchronisieren; gestörte Signalübertragung verändert die Anhaftung oder fördert übermäßige Invasion. Epigenetische Modifikationen und Dynamiken von Transkriptionsfaktoren verändern schnell die Genexpressionsprofile in sowohl embryonalen als auch maternalen Zellen und ermöglichen den Übergang von Adhäsion zu Invasion und Immunmodulation. Immunzellen an der Schnittstelle, wie uterine natürliche Killerzellen, reagieren auf molekulare Signale, formen die vaskuläre Anpassung und begrenzen schädliche Entzündungen. Diese zelluläre und molekulare Choreographie garantiert, dass die Einnistung erfolgt, wenn die Embryokompetenz und die mütterliche Bereitschaft übereinstimmen.
Veränderungen im Endometrium während der Implantation
Nun betrachten Sie, wie sich das Endometrium umgestaltet, um ein Embryo aufzunehmen, beginnend mit strukturellen Veränderungen wie Drüsen- und Epithelveränderungen. Sie werden sehen, wie Stromazellen eine Dezidualisierung durchlaufen, um die Implantation zu unterstützen. Außerdem behandeln Sie die Gefäßumlagerung und immunologische Anpassungen, die eine rezeptive, schützende Umgebung schaffen.
Endometriumstrukturveränderungen
Wenn der Blastozyst ankommt, verändert sich das Endometrium von einer proliferativen, östrogengetriebenen Schleimhaut zu einem sekretorischen, progesterondominierten Gewebe, das darauf vorbereitet ist, die Implantation aufzunehmen und zu unterstützen. Sie bemerken Veränderungen in der Endometriumsdicke, während sich die Drüsen verlängern und sich spiralig winden, wodurch die sekretorische Oberfläche und die Nährstoffverfügbarkeit zunehmen; die Gefäßnetze weiten sich aus, sodass der Blutfluss den Bedürfnissen des Embryos entspricht. Das luminale Epithel wird empfänglicher, mit veränderter Zellpolarität und verringerten adhäsiven Barrieren, die es dem Blastozysten erlauben, sich anzulagern. Die stromalen Kompartimente reorganisieren ihre extrazelluläre Matrix, indem sie Kollagen- und Glykoproteinzusammensetzung modifizieren, um eine kontrollierte Invasion zu ermöglichen, ohne dass es zu einem großflächigen Gewebeabbau kommt. Lymphozyten- und Makrophagenpopulationen verteilen sich neu, um die lokale Immuntoleranz zu modulieren. Diese strukturellen Veränderungen, die durch präzise hormonelle Einflüsse gesteuert werden, bereiten die Bühne für ein stabiles Einbetten des Embryos, ohne dabei bereits die stromale deku- duale Umwandlung zu beschreiben.
Dezidualisierung von Stromazellen
Obwohl sie dem strukturellen Umbau folgt, den Sie bereits gesehen haben, verwandelt die Dezidualisierung stromale Fibroblasten in spezialisierte, sekretorische Dezidua-Zellen, die die Embryoinvasion unterstützen und regulieren. Sie beobachten den Dezidualisierungsprozess, wie Zellen sich vergrößern, Glykogen und Lipide speichern und Zytokine sowie Wachstumsfaktoren sezernieren, die das implantierende Embryo leiten. Diese stromale Umwandlung polstert den Keimling, kontrolliert das Eindringen des Trophoblasten und schafft ein nährendes Mikroklima. Sie spüren sowohl Präzision als auch Verletzlichkeit in diesen Veränderungen: Timing und molekulare Signale müssen für eine erfolgreiche Implantation übereinstimmen. Unten steht eine einfache Tabelle, die dieses empfindliche Gleichgewicht hervorruft.
| Schutz | Signal | Hingabe |
|---|---|---|
| Erweichter Stroma | Dezidualisierungsprozess | Kontrollierte Invasion |
| Nährstoffspeicher | parakrine Signale | mütterliche Aufnahme |
Gefäß- und Immunanpassungen
Während sich der Embryo einnistet, remodeliert das Endometrium seine Blutversorgung und seine Immunlandschaft, um neuen metabolischen und defensiven Anforderungen gerecht zu werden; man beobachtet, dass sich die Spiralarterien weiten und tortuoser werden, während sich die dezidualen Immunzellen in Richtung Toleranz und kontrollierter Entzündung verschieben. Es tritt eine gezielte vaskuläre Umgestaltung auf, die den Blutfluss erhöht, den Widerstand senkt und eine Übergangszone schafft, die den Nährstoffaustausch unterstützt. Gleichzeitig werden lokale angeborene und adaptive Immunpopulationen — NK-Zellen, Makrophagen, regulatorische T-Zellen — umprogrammiert, um Immuntoleranz zu fördern, ohne Pathogene zu eliminieren. Zytokine, Wachstumsfaktoren und Matrixveränderungen koordinieren das Gefäßwachstum und stabilisieren die maternalfetale Schnittstelle. Wenn diese Prozesse fehlschlagen, besteht das Risiko einer schlechten Plazentation, Entzündung oder eines Schwangerschaftsverlusts; erfolgreicher Implantation hängt daher von zeitlich genau abgestimmter vaskulärer Umgestaltung und robuster Immuntoleranz ab, die zusammenarbeiten.
Embryonalentwicklung und Implantationskompetenz
Als Nächstes betrachten Sie, wann ein Embryo in die Lage kommt, sich einzunisten, mit dem Schwerpunkt auf dem Zeitpunkt des Erwerbs der Kompetenz. Sie untersuchen wichtige zelluläre und molekulare Marker, die Bereitschaft signalisieren. Außerdem setzen Sie diese Veränderungen in Beziehung zum empfänglichen Fenster der Gebärmutter, um zu zeigen, wie Embryo und Endometrium aufeinander abgestimmt sein müssen.
Kompetenzerwerbszeitpunkt
Wenn ein Säugetier-Embryo das Stadium erreicht, in dem er sich an die Gebärmutterschleimhaut anlagern und in diese eindringen kann, sagen wir, er habe Implantationskompetenz erworben; dieser Wechsel spiegelt zeitlich strikt abgestimmte Veränderungen in der Genexpression, der Zellpolarität und der Signalübertragung wider, die die Blastozyste darauf vorbereiten, mit mütterlichem Gewebe zu interagieren. Sie überwachen den Zeitpunkt des Kompetenzerwerbs, indem Sie Entwicklungsmeilensteine beobachten und Kompetenzbewertungsrahmen verwenden, die Morphologie und Embryonalalter mit einem empfänglichen Fenster verknüpfen. Präzises Timing ist wichtig: Wenn Sie den Transfer zu früh oder zu spät versuchen, sinken die Implantationschancen. Klinische und experimentelle Protokolle ordnen deshalb das Embryonalstadium der Uterusrezeptivität zu. Verwenden Sie die folgende Tabelle, um typische Stadien und praktische Hinweise zu vergleichen, damit Sie Eingriffe planen oder Ergebnisse effizient interpretieren können.
| Stadium | Praktischer Hinweis |
|---|---|
| Frühe Blastozyste | Morphologie prüfen |
| Expandierte Blastozyste | Ideales Transferfenster |
| Schlüpfende Blastozyste | Hohe Anlagerungspotenz |
| Nach dem Schlüpfen | Vermindertes Risiko der Desynchronisation |
Zelluläre und molekulare Marker
Das Wissen um den Zeitpunkt des Erwerbs von Fertigkeit (Competence) hilft Ihnen, die molekularen Signale zu interpretieren, die die Bereitschaft zur Implantation kennzeichnen. Sie werden nach spezifischen zellulären und molekularen Markern suchen, die ein kompetentes Embryo anzeigen: Trophoblastdifferenzierung, Polarität und metabolische Umstellungen. Änderungen in zellulären Signalwegen wie MAPK und PI3K/AKT verändern Adhäsions- und Invasionsfähigkeit. Gleichzeitig sagen dynamische Genexpressionsmuster — Transkriptionsfaktoren wie Oct4, Cdx2 und Gene, die Integrine und Proteasen regulieren — das Anlagerungspotenzial voraus. Sie werden epigenetische Marker und MicroRNA-Profile beurteilen, die diese Programme feinabstimmen. Funktionelle Assays zur Messung von Calciumflüssen, Kinasenaktivität oder sekretierter Faktoren können die Kompetenz über statische Marker hinaus bestätigen. Die gemeinsame Interpretation dieser Daten hilft Ihnen, die Implantationswahrscheinlichkeit abzuschätzen und zu entscheiden, ob Embryonen klinischen oder wissenschaftlichen Kriterien genügen.
Uterine Receptivity Window auf Deutsch: „Fenster der Gebärmutterempfänglichkeit“
Obwohl der Embryo für die Implantation kompetent sein muss, hängt eine erfolgreiche Anheftung auch von einem eng begrenzten Zeitfenster der Uterus-Rezeptivität ab, in dem das Endometrium die richtige Kombination aus Hormonen, Adhäsionsmolekülen und Immunmodulatoren exprimiert. Sie müssen erkennen, dass dieses Fenster – typischerweise die Tage 19–23 eines 28‑tägigen Zyklus – eine kurze Periode schafft, in der die Schleimhaut am gastfreundlichsten ist. Wenn die Uterusgesundheit durch Entzündungen, Fibrose oder veränderten Blutfluss beeinträchtigt ist, verringern Sie die Implantationschancen. Hormonelles Gleichgewicht, insbesondere Progesteron nach dem Eisprung, steuert die Stromadezidualisierung und die Expression von Pinopoden, die die Anhaftung erleichtern. Immunzellen passen sich an, um den Embryo zu tolerieren und gleichzeitig vor Krankheitserregern zu schützen. Klinisch beurteilen Sie das Fenster durch Endometriumdatierung, molekulare Tests oder Rezeptivitätstests, um den Embryotransfer zu timen oder modifizierbare Probleme anzugehen.
Frühe Anzeichen und Symptome der Einnistung
Da die Implantation normalerweise vor dem erwarteten Ausbleiben der Periode erfolgt, können ihre frühen Anzeichen subtil und leicht zu übersehen sein. Sie könnten leichte Schmierblutungen oder Krämpfe bemerken, etwa zu der Zeit, in der sich der Embryo einnistet, oft milder als Menstruationskrämpfe. Zu den frühen Schwangerschaftsanzeichen können Brustempfindlichkeit, leichte Übelkeit und ein leichter Anstieg der Basaltemperatur gehören. Hormonelle Veränderungen können bereits vor einem positiven Test Müdigkeit, Stimmungsschwankungen oder vermehrtes Wasserlassen verursachen.
| Anzeichen | Typischer Zeitpunkt | Was zu erwarten ist |
|---|---|---|
| Schmierblutung | 6–12 Tage nach dem Eisprung | Rosa oder braun, kurz |
| Krämpfe | Gleicher Zeitraum | Mild, von kurzer Dauer |
| Brustveränderungen | 1–2 Wochen nach dem Eisprung | Empfindlichkeit, Spannungsgefühl |
| Müdigkeit/Stimmung | Frühe Lutealphase | Müdigkeit, Reizbarkeit |
Diese Anzeichen überschneiden sich mit prämenstruellen Symptomen, daher sind sie nicht eindeutig. Wenn Sie eine Implantation vermuten, warten Sie mit einem Test bis zum Ausbleiben der Periode für verlässlichere Ergebnisse oder konsultieren Sie Ihre Ärztin bzw. Ihren Arzt für Rat.
Faktoren, die eine erfolgreiche Implantation fördern
Wenn Sie möchten, dass die Einnistung gelingt, konzentrieren Sie sich darauf, die richtigen hormonellen, uterinen und lebensstilbedingten Bedingungen zu schaffen: Ein rechtzeitiger Progesteronanstieg in der Lutealphase bereitet das Endometrium vor, eine empfängliche Gebärmutterschleimhaut mit ausreichender Durchblutung und einem ausgewogenen Immunsystem ermöglicht die Anheftung des Embryos, und gesunde Gewohnheiten – ausreichende Ernährung, kontrollierter Stress, Vermeidung von Rauchen und übermäßigem Alkohol – unterstützen die allgemeine Fruchtbarkeit. Sie fördern die Einnistung, indem Sie das hormonelle Gleichgewicht durch regelmäßige Zyklen erhalten und bei Bedarf ärztliche Unterstützung für Progesteron oder andere Behandlungen in Anspruch nehmen. Optimieren Sie die uterine Gesundheit durch das Management von Beschwerden wie Myomen oder Polypen und sorgen Sie für eine gute Durchblutung des Beckens; Ihr Clinician kann bildgebende Verfahren oder kleinere Eingriffe empfehlen, um strukturelle Probleme zu beheben. Achten Sie auf Lebensstilfaktoren: essen Sie eine nährstoffreiche Ernährung, halten Sie ein gesundes Gewicht, treiben Sie mäßig Sport, schlafen Sie ausreichend und minimieren Sie Schadstoffe. Reduzieren Sie Stress mit Techniken, die für Sie funktionieren, da chronischer Stress Hormone stören kann. Schließlich befolgen Sie den Rat Ihres Gesundheitsversorgers zur zeitlichen Abstimmung von Geschlechtsverkehr oder Schritten der assistierten Reproduktion, um das Embryonalstadium mit der optimalen Empfänglichkeit der Gebärmutterschleimhaut in Einklang zu bringen.
Ursachen und Folgen des Implantationsversagens
Sie haben Maßnahmen ergriffen, um das hormonelle Gleichgewicht, die Gebärmutterumgebung und den Lebensstil zu verbessern, doch die Einnistung kann aus vielen Gründen weiterhin fehlschlagen. Sie können auf Einnistungsprobleme stoßen durch genetische Anomalien des Embryos, eine schlechte Endometriumrezeptivität, strukturelle Gebärmutterveränderungen wie Myome oder Verwachsungen und immunologische Faktoren, die die Haftung stören. Hormonelle Einflüsse bleiben entscheidend: unzureichendes Progesteron, Lutealphasendefekte oder Schilddrüsenfunktionsstörungen können die richtige Umwandlung des Endometriums und die Unterstützung des Konzepts verhindern.
Wenn die Einnistung fehlschlägt, können Sie einen frühen Schwangerschaftsverlust, wiederholte Einnistungsschwierigkeiten oder eine verzögerte Empfängnis erleben, die emotionalen und finanziellen Druck erhöht. Wiederholtes Versagen kann eine weitergehende Abklärung erforderlich machen, die Behandlungsplanung beeinflussen und Entscheidungen zur assistierten Reproduktion nach sich ziehen. Sie sollten wissen, dass zu den Folgen auch veränderte uterine Signalübertragungen und mögliche Veränderungen der anschließenden Embryo‑Endometrium‑Interaktionen gehören. Obwohl nicht alle Ursachen reversibel sind, hilft die Identifizierung spezifischer Faktoren dabei, Maßnahmen und Beratung zu priorisieren, damit Sie fundierte Entscheidungen über die nächsten Schritte und Erwartungen treffen können.
Klinische Erkennung und Behandlung von Implantationsproblemen
Wenn bei Ihnen Probleme mit der Implantation vermutet werden, wird Ihr Kliniker die klinische Vorgeschichte, gezielte Tests und bildgebende Verfahren kombinieren, um wahrscheinliche Ursachen zu identifizieren und die Behandlung zu steuern. Sie besprechen Menstruationsmuster, frühere Schwangerschaften, Operationen, Infektionen und Lebensstilfaktoren. Zu den gezielten Tests gehören Hormonprofile, Thrombophilie-Screenings, die Beurteilung der Gebärmutterhöhle mittels Ultraschall oder Hysteroskopie sowie gegebenenfalls eine Endometriumbiopsie. Fortgeschrittene Bildgebung oder 3D-Ultraschall können strukturelle Anomalien aufzeigen, die zu Implantationsstörungen beitragen.
Die Behandlung hat Priorität auf maßgeschneiderten, evidenzbasierten klinischen Interventionen. Werden strukturelle Läsionen gefunden, stellt eine operative Hysteroskopie häufig die Integrität der Höhle wieder her. Hormonelle Ungleichgewichte werden mit geeigneter endokriner Therapie korrigiert; in der assistierten Reproduktion kann eine Lutealunterstützung eingesetzt werden. Antikoagulative oder immunmodulierende Ansätze sind spezialisierten, testbestätigten Situationen vorbehalten. Ihnen wird eine reproduktionsmedizinische Beratung angeboten sowie ein schrittweiser Plan, der Nutzen, Risiken und Zeitrahmen abwägt. Folgeuntersuchungen mit Bildgebung und Neubewertung bestätigen die Antwort, und bei komplexen medizinischen oder reproduktionschirurgischen Fällen steht eine multidisziplinäre Überweisung zur Verfügung.